تم النشر بواسطة روب باكارد on 28 حزيران، 2023
لم تتغير متطلبات التنسيق والمحتوى لتقديم FDA المسبق ، لكن إطلاق FDA PreSTAR غيّر كل شيء.
[المحتوى جزءا لا يتجزأ]
ما هو التقديم المسبق من إدارة الغذاء والدواء؟
يهدف التقديم المسبق لـ FDA إلى الحصول على إجابات للأسئلة التي لديك حول تقديم FDA في المستقبل. قد يتكون التقديم المسبق من مستند PDF كبير أو مستندات PDF متعددة. في التقديم المسبق الخاص بك ، يجب عليك تحديد إما استجابة بريد إلكتروني أو استجابة بريد إلكتروني من خلال مؤتمر عبر الهاتف. تتمثل إحدى ميزات اختيار مؤتمر عبر الهاتف في أنه يمكنك طرح أسئلة توضيحية خلال مؤتمر عبر الهاتف مدته ساعة واحدة مع إدارة الغذاء والدواء ، لكنك مسؤول عن تقديم مسودة محضر الاجتماع إلى إدارة الغذاء والدواء في غضون 15 يومًا من الاجتماع الهاتفي. إذا حددت ردًا عبر البريد الإلكتروني ، فلن تحتاج إلى تقديم محاضر الاجتماع إلى إدارة الغذاء والدواء. في الخامس من تموز (يوليو) 5 ، سنبدأ سلسلة ندوات عبر الإنترنت جديدة مكونة من 2023 أجزاء من إدارة الغذاء والدواء قبل التقديم. سيكون هذا هو التدريب النهائي قبل تقديم FDA. لا تفوتها.
ما هو الفرق بين التقديم المسبق لـ FDA وتقديم Q؟
يعد كل إرسال مسبق من قِبل إدارة الغذاء والدواء (FDA) عبارة عن تقديم Q ، ولكن ليست كل عمليات إرسال Q هي عمليات إرسال مسبقة. يقتصر نموذج PreSTAR الجديد حاليًا على التقديم المسبق لـ FDA ، ولكن سيتم توسيع القالب إلى أنواع أخرى من Q-subs لاحقًا. نموذج FDA قبل التقديم (على سبيل المثال ، PreSTAR) الإصدار التجريبي 0.1 غير ضروري للردود على أسئلة المراجعة التفاعلية من إدارة الغذاء والدواء. ما عليك سوى إرسال بريد إلكتروني إلى المحكم الرئيسي (الحد الأقصى لحجم الملف هو 25 ميغابايت للبريد الإلكتروني).
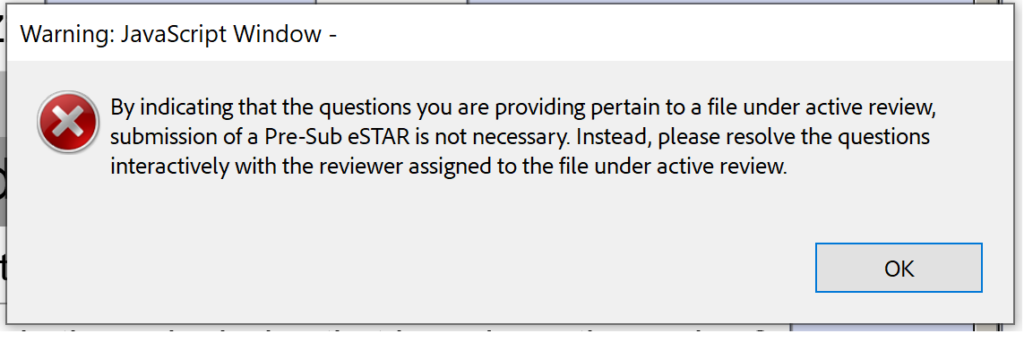
لسوء الحظ ، الإصدار التجريبي 0.1 ليس جاهزًا أيضًا لاجتماعات التقديم قيد المراجعة (SIR) أو الردود على IDE أثناء المراجعة التفاعلية.
13 نوعًا آخر من عمليات الإرسال قد تستفيد من عمليات إرسال Q:
- طلبات إصدار التقديم (SIRs)
- دراسة تحديد المخاطر
- اجتماعات إعلامية
- طلبات التعيين المتقدمة للأجهزة
- اجتماعات إعلامية
- يوم 100 اجتماعات سلطة النقد الفلسطينية
- اجتماعات الاتفاق والحسم
- التقديمات المرتبطة ببرنامج STeP
- طلبات تصنيف الملحقات
- طلبات الحصول على تعليقات إدارة الغذاء والدواء بشأن أسئلة محددة أو مسائل السياسة الشاملة
- طلبات الاعتراف بقواعد بيانات المتغيرات الجينية المتاحة للجمهور
- الجمع بين اجتماعات اتفاقية المنتج (CPAM) ، و
- ردود الفعل على ملاحظات التفتيش 483 إدارة الغذاء والدواء.
نتوقع أن يكون نموذج PreSTAR متاحًا في النهاية لطلب 513 (g) في المستقبل لأنه تم التحقق من صحته بالفعل لهذا الغرض.
ما هو رقم تقديم Q؟
يتم تعيين رقم مستند يبدأ بحرف "Q" لجميع عمليات إرسال Q عند الاستلام (أي Qyyxxxx). يتكون تنسيق الرقم من رقمين (على سبيل المثال ، "yy") لسنة التقديم (على سبيل المثال ، "2" لعام 23) و 2023 أرقام (أي "xxxx") وهي الرقم التسلسلي التالي المعين بواسطة إدارة الغذاء والدواء (FDA) لتلك السنة التقويمية. لذلك ، فإن أول طلب Q- استلمته إدارة الغذاء والدواء في يناير 4 هو Q2023 ، وعادة ما يتم استلام ما بين 230001 و 3,500 طلب جديد كل عام. إذا تم إرسال الجهاز الموضوع في إرسال Q سابق ، فسيتم إعادة استخدام رقم المستند الأصلي ، ويتم إضافة رقم إضافي (على سبيل المثال ، Qyyxxx / S4,000 ، Qyyxxx / S001 ، إلخ). يتم شرح ترقيم إرسال Q بمزيد من التفصيل في ملف 2023 توجيهات إدارة الغذاء والدواء.
هل تتقاضى إدارة الغذاء والدواء (FDA) رسوم تقديم Q؟
لا تتطلب التقديمات المسبقة لـ FDA دفع رسوم مستخدم FDA (أي 0 دولار).
كم من الوقت يستغرق التقديم المسبق من إدارة الغذاء والدواء؟
لقد ولت أيام سحق الجداول الزمنية. الجدول الزمني هو 70-75 أيام التقويم. في 5 أكتوبر 2022 ، MDUFA الخامس تم قبوله. كأحد أهداف القرار MDUFA V ، تم تكليف إدارة الغذاء والدواء بتقليل الجدول الزمني للرد على الأسئلة الفرعية الفرعية في غضون 70 يومًا لـ 90٪ من الطلبات المسبقة. تم تكليف إدارة الغذاء والدواء الأمريكية (FDA) بتحقيق هذا الهدف بحلول مارس 2024. إذا نجحت ، فستتلقى إدارة الغذاء والدواء زيادة قدرها 59 موظفًا في ميزانيتها في عام 2024. هذا ما يقرب من 19 مليون دولار حافز للرد على أسئلة اجتماع ما قبل التقديم في غضون 70 أيام. لتعكس أهداف القرار MDUFA V الجديدة هذه ، قامت FDA بتحديث ملف دليل Q-Sub المستند ليعكس التاريخ المستهدف وهو 70 يومًا لاستجابة البريد الإلكتروني و 75 يومًا للاجتماعات عبر الهاتف. قامت إدارة الغذاء والدواء أيضًا بتحديث بوابة تعاون العملاء (CCP) لتسهيل تتبع المواعيد النهائية للتقديم من قبل إدارة الغذاء والدواء.
ما هي FDA PreSTAR؟
في الماضي ، كان عليك إنشاء مستند (مستندات) خاص بك لتقديم FDA مسبقًا. يقوم بعض الأشخاص بإنشاء مستند PDF كبير مقسم إلى أقسام ، بينما يقوم الآخرون بإنشاء مستندات PDF منفصلة لكل متطلب من إرشادات ما قبل التقديم الخاصة بـ FDA. في 6 يونيو 2023 ، أصدرت إدارة الغذاء والدواء نسخة تجريبية (أي ، إصدار 0.1) لقالب PDF جديد (على سبيل المثال ، FDA PreSTAR). يوفر قالب PreSTAR الجديد هذا مزايا متعددة لإدارة الغذاء والدواء:
- كل شركة تستخدم نفس التنسيق ،
- يتحقق النموذج تلقائيًا من أن الإرسال المسبق يتضمن جميع العناصر المطلوبة ، و
- سيشجع تضمين العناصر الاختيارية الشركات على تقديم تفاصيل أكثر عن الأجهزة التي قد توفرها بخلاف ذلك.
كما يفيد PreSTAR المقدمين:
- لن تنسى أبدًا العناصر المطلوبة للتقديم المسبق لـ FDA ،
- لن تضطر أبدًا إلى التحقق من صحة نسخة FDA الإلكترونية ، و
- سوف يدربك التنسيق المماثل وواجهة المستخدم على استخدام FDA eSTAR.
ملاحظة: 1 أكتوبر 2023 هو الموعد النهائي لتنفيذ FDA eSTAR.
هل يجب عليك استخدام قالب PreSTAR؟
لا. الإصدار 0.1 من PreSTAR هو إصدار تجريبي واختياري بنسبة 100٪. ومع ذلك ، فأنا أحبه أفضل من القوالب الخاصة بي. لا يزال بإمكان فريق التصميم لديك الاحتفاظ بمستندات فردية لدليل المستخدم ووصف الجهاز وخطة الاختبار. نرفق المستند باستخدام الزر الذي يقول "إضافة مرفق" (انظر لقطة الشاشة أدناه).

تم تصميم قالب PreSTAR بواسطة Patrick Macatangga ، وهو مهندس أدوات وقوالب يعمل في FDA في فريق Lifecycle Tools and Templates. للمساعدة في تحديد مكان توجيه الأسئلة حول النموذج ، اقترح:
- إذا كانت لديك أسئلة أو تعليقات بخصوص الاستخدام الطوعي لـ eSTAR للأجهزة الطبية التي ينظمها CDRH ، أو إذا كانت لديك أسئلة عامة حول الأجهزة الطبية ، فيرجى الاتصال بـ شعبة الصناعة وتعليم المستهلك (DICE).
- إذا وجدت أي أعطال أو أخطاء في نموذج eSTAR للأجهزة الطبية التي ينظمها CDRH ، فيرجى الاتصال [البريد الإلكتروني محمي].
- إذا كانت لديك أسئلة بخصوص 510 (k) s أو طلبات De Novo أو طلبات التقديم المبكر للأجهزة الطبية التي ينظمها CDRH ، فيرجى الاتصال [البريد الإلكتروني محمي].
كيف ترسل eCopy؟
يمكنك إرسال نسخة إلكترونية من FDA على وسائط إلكترونية (على سبيل المثال ، محرك أقراص فلاش USB) وإرسالها عبر FedEx إلى مركز مستندات FDA على العنوان التالي: إدارة الغذاء والدواء ، مركز الأجهزة والصحة الإشعاعية ، مركز توثيق البريد ، 10903 New Hampshire Ave. ، Bldg. 66 ، جمهورية مقدونيا. G609، Silver Spring، MD 20993-0002. ومع ذلك ، يمكنك أيضًا إرسال FDA eCopy عبر مستعرض ويب (على سبيل المثال ، CCP ... انظر القسم التالي حول كيفية إرسال PreSTAR).
إذا كنت ترسل eCopy من خلال CCP بدلاً من FDA PreSTAR
كيف تقدم PreSTAR؟
لديك خياران لتسليم طلب FDA المسبق:
- احفظ العنصر الفرعي على الوسائط الإلكترونية (على سبيل المثال ، محرك أقراص فلاش USB) وأرسله عبر FedEx إلى إدارة الأغذية والعقاقير (FDA) ، و
- قم بتحميل العنصر الفرعي إلى بوابة تعاون العملاء الجديدة (CCP) الخاصة بإدارة الغذاء والدواء.
[المحتوى جزءا لا يتجزأ]
كما يمكنك أن تتخيل من الفيديو أعلاه ، فإننا نستخدم الخيار 2 فقط لتقديم الطلبات المسبقة من قِبل إدارة الأغذية والعقاقير (FDA). بالنسبة للخيار 2 ، يمكنك تحميل eCopy (محفوظ كملف مضغوط) أو PreSTAR (بتنسيق PDF الأصلي). توضح لك الصورة أدناه كيف يتم ذلك ، ولكن عملية التحميل تستغرق عادةً حوالي دقيقة واحدة - اعتمادًا على حجم الملف وعرض النطاق الترددي. أنت تستطيع تسجيل جديد لحساب CCP الخاص بك في ثوان.

ما هي عملية ما قبل التقديم؟
يعد إعداد وتحميل طلب اجتماع ما قبل التقديم الخاص بـ FDA هو الخطوة الأولى فقط من العملية. ستتلقى رسالة بريد إلكتروني تلقائية تؤكد أنه تم تحميل التقديم المسبق بنجاح ، وبعد ذلك ستتلقى خطابًا آليًا عبر البريد الإلكتروني يمنحك رقم Q-sub الذي تم تعيينه. ستتلقى أيضًا رسالة بريد إلكتروني آلية لإعلامك بقبول التقديم المسبق ، أو سيتصل بك مراجع إدارة الغذاء والدواء إذا كانت هناك حاجة للتغييرات. سيتصل بك مراجع إدارة الغذاء والدواء المعين عادة عن طريق البريد الإلكتروني خلال الأسابيع الثلاثة الأولى لجدولة مؤتمر عبر الهاتف إذا طلبت ذلك ، ولكن التاريخ / الوقت المعروض عادة لا يتطابق مع توفر فريق إدارة الغذاء والدواء ، وقد يتم تقديم تواريخ / أوقات بديلة.
ستتلقى ردًا عبر البريد الإلكتروني من إدارة الغذاء والدواء الأمريكية (FDA) لكل سؤال من أسئلتك في غضون 70 يومًا من استلام إدارة الغذاء والدواء. إذا طلبت عقد مؤتمر عبر الهاتف ، فسيكون عادةً حوالي 75 بعد استلام طلب اجتماع ما قبل التقديم من إدارة الغذاء والدواء. يحتاج فريقك إلى إعداد خطة مناقشة مفصلة لعقد مؤتمر عبر الهاتف مدته ساعة واحدة. يوصى بشدة باستخدام مجموعة الشرائح لتسهيل الاتصال ولكنها ليست مطلوبة. إذا قمت بتوفير مجموعة شرائح ، فيجب عليك إرسالها بالبريد الإلكتروني إلى المراجع قبل الاجتماع. ستحتاج أيضًا إلى تقديم نسخة من مجموعة الشرائح مع محضر اجتماعك. في بداية المؤتمر الهاتفي ، يجب أن يلتزم شخص من فريقك بإرسال مسودة محضر الاجتماع إلى إدارة الغذاء والدواء في غضون 15 يومًا. سترد إدارة الغذاء والدواء الأمريكية (FDA) بقبول محضر اجتماعك ، أو ستقدم نسخة معدلة. من الشائع أيضًا تقديم FDA مسبقًا مع بروتوكولات مفصلة وأسئلة جديدة إلى FDA.
نشر في: بريستار
- محتوى مدعوم من تحسين محركات البحث وتوزيع العلاقات العامة. تضخيم اليوم.
- PlatoData.Network Vertical Generative Ai. تمكين نفسك. الوصول هنا.
- أفلاطونايستريم. ذكاء Web3. تضخيم المعرفة. الوصول هنا.
- أفلاطون السيارات / المركبات الكهربائية ، كربون، كلينتك ، الطاقة، بيئة، شمسي، إدارة المخلفات. الوصول هنا.
- BlockOffsets. تحديث ملكية الأوفست البيئية. الوصول هنا.
- المصدر https://medicaldeviceacademy.com/fda-pre-submission/
